عالم الذرة
ممدوح عبد الغفور حسن
هيئة المواد النووية
نظرة تاريخية
أخذ الإنسان منذ زمن طويل يفكر فى تركيب المادة وما عساه أن يكون أصغر جزء فيها، وكيفية الوصول إليه، وحاول إبراز تصوراته فى تساؤل كالآتى: إذا أخذنا أى جزء من مادة صلبة وقسمناه نصفين، ثم أخذنا أحد النصفين وقسمناه إلى نصفين أيضا، ثم أخذنا أحد النصفين وقسمناه إلى نصفين، وكررنا العملية، فماذا ستكون النتيجة؟ اختلفت آراء الفلاسفة والعلماء القدامى فى الإجابة على هذا السؤال، ولكنها تبلورت فى رأيين اثنين: يرى أحدهما أن العملية ستستمر إلى ما لانهاية، ويرى الآخر أن استمرار عملية التقسيم سينتهى إلى مرحلة نهائية عند الوصول إلى أصغر جزء من المادة، وهو الجزء الذى لا يمكن تجزئته، وهو أصغر جزء يحتفظ بكل خواص هذه المادة. وقد أطلق العلماء العرب على هذا الجزء المادى غير القابل للتقسيم "الجوهر الفرد" واعتبروا أن كل مادة لها جوهرها الفرد الخاص بها، وأن أية مادة تتكون من تجمع أعداد كبيرة من الجوهر الفرد الخاص بها. وكان هذا المفهوم هو أول لبنة فى صرح النظرية الذرية للمادة. ثم وضع اللبنة الثانية العالم الانجليزى جون دالتون John Dalton فى نظريته الذرية التى بناها على مشاهداته فى تفاعل المواد مع بعضها، والتى عضَّدت مفهوم الجوهر الفرد الذى قال به العلماء العرب من قبل، وأصبح الجوهر الفرد يعرف حاليا باسم الذرة atom. وتم تعريف الذرة بناء على نظرية دالتون على أنها أصغر جزء من المادة، يحتفظ بكل خواص هذه المادة، وهو غير قابل للتجزئة. وتوالت البحوث العلمية فى طريق توضيح كنه هذا الجوهر الفرد، أو الذرة، ولا زالت تتوالى حتى الآن، فعالم الذرة، هذا العالم المتناهى فى الصغر، لا زالت تكتنفه الأسرار، ولا زال العلم يسعى حثيثا لاكتشافها.
ومن أهم اللبنات التى تبعت نظرية دالتون فى بناء فهم عالم الذرة هى إضافات العالم الدانيمركى نيلز بوهرNiels Bohr الذى وضع أسس النظرية الذرية الحديثة modern atomic theory والتى بينت أنه وإن كانت الذرة هى أصغر جزء من أى مادة يحتفظ بخواصها، إلا أن الذرة نفسها تتكون من جسيمات متعددة، وأن هذه الجسيمات هى نفسها فى جميع الذرات المختلفة، ولكن الاختلاف بين الذرات وبعضها هو فقط فى عدد هذه الجسيمات. ومنذ ذلك الوقت تراكمت المعلومات عن الذرة مما أدى إلى إطلاق الطاقة النووية، ولذلك فإن فهم الطاقة النووية والوقود النووى لابد وأن يبدأ بفهم جيد لتركيب الذرة، وهذا ما أهدف إليه فى هذا المقال.
هل الذرة أصغر جزء مادى؟
يقول لنا علم الكيمياء إن أية مادة فى الكون إما أن تكون عنصرا element أو تكون مركبا compound. والعنصر هو المادة التى لا يمكن تحليلها إلى مواد أبسط منها، فكل ذراته من نوع واحد فقط، أما المركب فهو المادة التى تتكون من التحام عدد من الذرات المختلفة لتكوِّن مايسمى الجزئmolecule ؛ فالمركب إذن هو الذى يتكون من اتحاد أكثر من عنصر، إثنين أو أكثر، ولهذا يمكن تحليل المركب أو تفكيكه إلى مواد أبسط منه، وهى العناصر الداخلة فى تركيبه. ونضرب لهذا مثالا؛ فالماء مركب يتكون كل جزئ من جزيئاته من اتحاد عنصرين هما الهيدروجين والأكسجين، حيث تتحد ذرتان من الهيدروجين مع ذرة واحدة من الأكسجين لتكون جزىء الماء؛ ولذلك نستطيع بوسائل معينة تحليل الماء إلى هيدروجين وأكسجين، ولكن لا يمكن تحليل الهيدروجين إلى مواد أبسط، وكذلك الأكسجين. مثال آخر وهو ثانى أكسيد الكربون؛ فكل جزئ من هذا الغاز يتكون من اتحاد ذرة واحدة من الكربون مع ذرتين من الأكسجين. نستطيع إذن أن نقرر بكل الثقة أن العنصر يتكون من ذرات من نوع واحد فقط، أما المركب فهو يتكون من جزيئات متشابهة، وكل جزئ بدوره يتكون من التحام عدة ذرات مختلفة، اثنتين أو أكثر، مع بعضها.
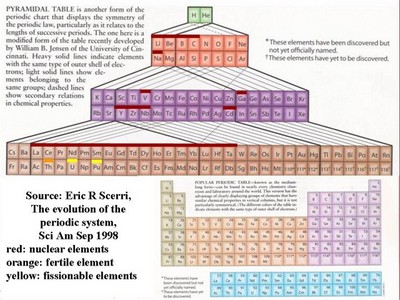
ومن التعاون بين علمى الكيمياء والفلك تبين لنا أن عدد عناصرالأرض كلها 92 عنصرا فقط، أما المركبات فلا حصر لها. وقد تم ترتيب هذه العناصر حسب ثقل أنويتها فى جدول يعرف باسم الجدول الدورى للعناصر periodic table of the elements يبدأ بالهيدروجين وهو أخف العناصر وأبسطها من ناحية تكوين ذراته، وينتهى باليورانيوم وهو أثقل العناصر وأكثرها تعقيدا من ناحية تركيب ذراته (شكل 1 الجدول الدورى للعناصر). وقد وُجِدَ أن خصائص العناصر ترتبط إلى حد كبير بوضعها فى ذلك الجدول.
ومن التطورات العلمية المتتابعة فى الربع الأول من القرن العشرين، تبين أن ذرات جميع المواد بلا استثناء تتكون من ثلاثة جسيمات particles رئيسية تم اكتشافها واحدا تلو الآخر، وهى: النيوترون neutron وهو جسيم متعادل الشحنة، والبروتون proton وهو جسيم يحمل شحنة كهربية موجبة وتبلغ كتلته مثل كتلة النيوترون تقريبا، والإلكترون electron وهو جسيم يحمل شحنة كهربائية سالبة تعادل فى مقدارها شحنة البروتون ولكن كتلته تعادل جزء من 1480 جزء من كتلة البروتون أو النيوترون (شكل 2 مكونات الذرة). وفى أية ذرة تتجمع البروتونات والنيوترونات مع بعضها فى مركز الذرة لتكون كتلة مركزية تعرف باسم النواة nucleus، أما الإلكترونات فإنها تسبح حول هذه النواة على أبعاد شاسعة جدا على المستوى الذري. ولكى تكون الذرة متعادلة كهربائيا لابد من أن يكون عدد بروتوناتها فى النواة مساويا لعدد الإلكترونات التى تسبح حول هذه النواة. ولبيان ذلك سنذكر بعض الأمثلة: نأخذ أولا ذرة الهيدروجين، الذى يحتل المركز الأول فى الجدول الدورى، فذرة الهيدروجين تحتوى على بروتون واحد فقط، وهو الذى يكون النواة، ويسبح حوله إلكترون واحد فقط؛ لذلك فهى أبسط الذرات، وهى الذرة الوحيدة بين كل أنواع الذرات التى لا تحتوى نواتها على نيوترونات، ولذلك إذا ذكرنا نواة ذرة الهيدروجين فإننا نعنى أيضا البروتون. ثم يأتى بعد ذلك الهيليوم الذى يحتل المركز الثانى فى الجدول الدورى للعناصر وتحتوى نواة ذرته على بروتونين ونيوترونين، ويسبح حول هذه النواة إلكترونان. وإذا ذهبنا إلى العنصر الذى يحتل المركز الثالث فى الجدول الدورى نجده الليثيوم lithium، وهو من الفلزات القلوية وتحتوى نواته على ثلاثة بروتونات وثلاثة نيوترونات. وإذا أخذنا العنصر الرابع، وهو البريليوم، نجد أن نواته تحتوى على أربعة بروتونات وأربعة نيوترونات... وهكذا نجد أن ترتيب العناصر فى الجدول الدورى يتصاعد بزيادة بروتون لكل عنصر تالٍ حتى نصل إلى اليورانيوم الذى يحتل المركز الثانى والتسعين فى الجدول الدورى ونجد أن نواته تحتوى على 92 بروتونا. وعلى هذا نجد أن عدد البروتونات فى نواة أى عنصر هو الذى يحدد موقع هذا العنصر فى الجدول الدورى وهو الذى يحدد هوية هذا العنصر، ولا يوجد عنصران مختلفان يحملان نفس عدد البروتونات فى النواة؛ ولذلك يعتبر عدد البروتونات فى نواة أى عنصر بمثابة رقم بطاقته الشخصية التى لا يشاركه فيها أى عنصر آخر، أو بصمته التى ينفرد بها، ويطلق عليه تعبير الرقم الذرى atomic number للعنصر، وإذا تغير هذا الرقم فإن هوية العنصر تتغير إلى العنصر المقابل للرقم الجديد.
ولكن ماذا عن النيوترونات والإلكترونات؟ نتناول النيوترونات أولا. مع التصاعد فى الجدول الدورى مع الرقم الذرى نجد أن عدد النيوترونات يساوى عدد البروتونات فى أنوية العناصر حتى العنصر رقم 8 وهو الأكسجين؛ حيث تحتوى نواته على 8 بروتونات و 8 نيوترونات، ولكن بعد الأكسجين نجد أن عدد النيوترونات يزيد عن عدد البروتونات بمقدار يتزايد مع الرقم الذرى حتى يصل إلى 146 نيوترونا فى نواة ذرة اليورانيوم، وحيث أن كتلة الإلكترون أقل بكثير من كتلة كل من النيوترون والبروتون، فإن كتلة الذرة تتركز أساسا فى نواتها، وإذا أخذنا كتلة النيوترون كوحدة لتقدير كتلة النواة يصبح مجموع عدد البروتونات والنيوترونات مساويا لكتلة الذرة، مع إهمال كتلة الإلكترونات، ولقد اصطلح على تسمية هذا العدد بالوزن الذرى atomic weight للعنصر. ولتوضيح هذا الأمر نأخذ ذرة الهيدروجين مرة أخرى كمثال؛ فهى تـتكون مـن بروتـون واحد فقــط فى النواة وإلكترون واحد فقـط يسبح حوله، وبذلك يكون العدد الذرى للهيدروجين واحدا والوزن الذرى أيضا واحدا. وفى ذرة الأكسجين تحتوى النواة على ثمانية بروتونات وثمانية نيوترونات وتسبح حولها ثمانية إلكترونات، ولهذا يكون الرقم الذرى للأكسجين 8 والوزن الذرى له 16. أما ذرة اليورانيوم فنواتها تحتوى على 92 بروتونا و146 نيوترونا، ويسبح حولها 92 إلكترونا، ولهذا فالرقم الذرى لليورانيوم هو 92، ووزنه الذرى هو 238 (92+146).
ومن الأمور الشائعة فى العناصر أن بعض الأنوية تحتوى على عدد أكبر أو أقل قليلا من النيوترونات عن العدد الموجود فى معظم ذرات العنصر؛ فنواة الأكسجين كما قلنا تحتوى على ثمانية بروتونات وثمانية نيوترونات ووزنها الذرى 16، وهذا هو الشائع، ومع ذلك توجد بعض ذرات الأكسجين التى تحتوى نواتها على عشرة نيوترونات بدلا من ثمانية فقط، وبهذا يصبح وزنها الذرى 18 وليس 16، ولذلك يقال إن للأكسجين نظيرين، بمعنى توأمين، أحدهما "الأكسجين16" وهو الشائع، والآخر يسمى "الأكسجين18" ويشكل حوالى 0.2% من مجموع ذرات الأكسجين. والفرق الوحيد بين هذين النظيرين للأكسجين أن أحدهما أثقل من الثانى بمقدار ضئيل جدا. وجميع العناصر لها نظائر إما واحدا أو أكثر، بيد أن أحد هذه النظائر هو الذى يشكل الغالبية العظمى للعنصر.
وبعد أن تكلمنا عن النيوترونات نأتى للكلام عن الإلكترونات التى تسبح حول النواة وعددها يساوى عدد البروتونات القابعة فى النواة ولهذا تكون الذرة فى مجموعها متعادلة كهربائيا، وتسبح هذه الإلكترونات حول النواة بطريقة منتظمة تحكمها قواعد معينة تبين أنها تحتل مدارات ذات أشكال معقدة ولا يمكن رسمها على هيئة دوائر أو أشكال بيضاوية حول النواة كما تصورها معظم الكتب والمراجع، وما ذلك إلا تبسيط مبالغ فيه ويعطى انطباعا غير حقيقى عن توزيع الإلكترونات حول النواة. وإمعانا فى التبسيط يحلو للبعض تشبيه الذرة بالمجموعة الشمسية فيشبهون النواة بالشمس ويشبهون الإلكترونات بالكواكب التى تدور حولها، إلا أن هذا التشبيه أمر ظاهرى فقط ويعطى انطباعا زائفا عن التركيب الحقيقى للذرة يجعل من الصعب على الإنسان أن يتابع تركيب الذرة على مستويات متقدمة لأن ذلك يستلزم منه التخلص من هذا الانطباع الكاذب؛ فمن المعروف أن القوانين التى تحكم الأجرام الكبيرة فى الكون، نستطيع بها قياس حركة أى جرم من الأجرام التى نرصدها ونسجل هذه الحركة بأجهزتنا ومن ذلك يمكن تحديد مكان هذا الجرم بدقة فى أى لحظة مستقبلية، ونستطيع أيضا أن نحدد بدقة الخط الذى سيسير فيه منذ لحظة القياس إلى أى لحظة مستقبلية، وبهذه القوانين يمكننا أيضا تحديد النقطة التى ستسقط فيها أى مقذوفة نطقلها فى ظروف معروفة؛ وهكذا أمكن غزو الفضاء والنزول على سطح القمر وإطلاق الأقمار الصناعية وتحديد مساراتها بدقة. أما إذا نزلنا إلى عالم الذرة، وهو العالم متناهى الصغر، فإن قوانين نيوتن أو أينشتين تخفق ولا تعترف بها الجسيمات الذرية، مثل الإلكترونات و البروتونات والنيوترونات، وسائر الجسيمات الذرية العجيبة، فهذه الجسيمات تعرف وتطيع قوانين أخرى ذات معادلات معقدة؛ لهذا فإن ديناميكية الذرة تختلف عن ديناميكية المجموعة الشمسية اختلافا جوهريا، ويحسن بنا أن نتلافى التبسيط المخل عند الحديث عن طبيعة الذرة، خاصة إذا كنا نخاطب الأطفال والشباب فى المراحل الدراسية المبكرة، حتى لا نعيق تفهمهم لطبيعة عالم الذرة فى المراحل الدراسية المتقدمة.
كذلك يمكن لأية ذرة أن تفقد إلكترونا أو أكثر من المدار الخارجى فتظهر عليها شحنة كهربائية موجبة مقدارها يعادل عدد الإكترونات التى فقدتها، وغالبا لا يزيد عدد هذه الإلكترونات عن أربعة، وفى هذه الحالة تسمى أيونا موجبا أو أنيونا anion وتجعل له نشاطا كيميائيا. ومن جهة أخرى يمكن فى ظروف معينة أن تفقد الذرة إلكترونا أو أكثر وتتحول بذلك إلى أيون سالب أوكاتيونا cation، وهذا يحدث مع الكثير من الفلزات ويؤدى إلى النشاط الكيميائى والقابلية للدخول فى تفاعلات كيميائية. ونتيجة لذلك يمكن أن يلتحم كاتيون وأنيون مع بعضهما نتيجة التجاذب الكهربى بينهما، مثال ذلك ملح الطعام الذى يتكون من كاتيون صوديوم ذى شحنة كهربائية واحدة موجبة مع أنيون كلور ذى شحنة كهربائية واحدة سالبة لتكوين جزئ من كلوريد الصوديوم الذى تختلف خصائصه كلية عن كل من الصوديوم والكلور، وهذه إحدى صور الالتحام بين العناصر برابطة تسمى الرابطة الأيونية ionic bond لتكوين المركبات التى تسمى المركبات الأيونية ionic compounds نظرا لتكونها من أيونات، وهناك طرق أخرى.
إلى هنا قد يتسائل القارئ: لماذا الخوض فى هذه المعلومات الأولية فى معرض حديثنا عن الوقود النووى والطاقة النووية؟ الغرض من هذا هو توضيح السبب فى إعطاء صفة النووية للوقود وللطاقة الناتجة عنه. وهذا ما سنبدأ بالدخول فيه بعد هذه المقدمة لنبين الفرق بين التفاعلات الكيميائية من جهة، و التفاعلات النووية، والفرق بين الاحتراق الكيميائى والاحتراق النووى، والفرق بين التفجير الكيميائى والتفجير النووى، وهى ثلاثة فروق هامة يجب فهمها كقاعدة لفهم الوقود النووى والطاقة النووية وبالتالى تكوين الثقافة النووية الشعبية مع شعب عليه أن يدخل العصر النووى.
التفاعل الكيميائى والتفاعل النووى
التفاعل الكيميائى هو التحام أو اتحاد العناصر لتكوين مركبات، أو تفكك المركبات إلى عناصرها، وكذلك كل التنوعات الأخرى لهذه التفاعلات، ودراسة هذه التفاعلات وخصائصها والظروف التى تجرى فيها هو مجال علم الكيمياء بصفة عامة، وتتم هذه التفاعلات عن طريق الإلكترونات فقط، ولا تشترك فيها النواة ولا تتأثر بها إطلاقا. ويمكن تمييز التفاعلات الكيميائية من ناحية الحرارة إلى نوعين: الأول يشمل التفاعلات الطاردة للحرارة exothermic reactions، وذلك لأن كمية الطاقة الحرارية فى المواد المتفاعلة أكثر منها فى نواتج التفاعل وهذا الفرق يظهر على هيئة طاقة حرارية منبعثة من نواتج التفاعل، أما النوع الثانى من التفاعلات الكيميائية فيشمل التفاعلات الماصة للحرارة endothermic reactions، أى التى تحتاج إلى إمداد من الحرارة لكى تتم وذلك لأن كمية الحرارة الكامنة فى نواتج التفاعل أكثر من الحرارة الكامنة فى المواد المتفاعلة. ومن خصائص التفاعلات الكيميائية أن كتلة المواد المتفاعلة تساوى كتلة المواد الناتجة عن التفاعل تطبيقا لقانون بقاء المادة الذى ينص على أن المادة لا تنعدم ولا تستحدث، ولكنها فقط تتغير من صورة إلى أخرى، ونفس الشئ يقال عن الطاقة فهى أيضا لا تنعدم ولا تستحدث ولكنها تتحول من صورة إلى أخرى، فلو أننا حسبنا كمية الطاقة المختزنة فى المواد المتفاعلة لأى تفاعل طارد للحرارة لوجدناها مساوية تماما للطاقة المختزنة فى المواد الناتجة عن التفاعل مضافا إليها الحرارة المنبعثة من التفاعل. وهكذا نجد أن التفاعلات الكيميائية تطيع قانونى بقاء المادة والطاقة. أما التفاعلات النووية فهى التفاعلات التى تمس نواة الذرة وتؤدى إلى تغيرات فيها وتقوم بها الجسيمات النووية، ولذلك أعطيت صفة النووية، وقد تشترك فيها بعض الإلكترونات فى بعض الحالات. والتفاعلات النووية هى أيضا إما تفاعلات طاردة للحرارة أو تفاعلات ماصة للحرارة مثل التفاعلات الكيميائية تماما، ولكنها تختلف جذريا عن التفاعلات الكيميائية فى أنها لا تطيع قانونى بقاء المادة والطاقة؛ ففيها يمكن تحويل الطاقة إلى مادة أو المادة إلى طاقة حسب معادلة النسبية المشهورة التى تنص على أن المادة والطاقة هما صورتين لنفس الشئ وأن كمية الطاقة، مقدرة بالجول، المقابلة لأية كمية من المادة تساوى كتلة هذه المادة مقدرة بالكيلوجرام مضروبة فى مربع سرعة الضوء مقــدرة بالمتر فى الثانية، والتى تبلــــــغ 300 ألف كيلــومتر فى الثانية؛ أى 9* 1610 متر/ثانية، وهذا رقم كبير جدا، ويعنى ذلك أن المادة ما هى إلا طاقة مركزة تركيزا متناهيا، ويعنى أيضا أنه يمكن الحصول على كميات هائلة من الطاقة من جزء صغير جدا من المادة إذا استطعنا أن نجبر المادة على أن تتحول إلى طاقة حسب معادلة النسبية المشهورة. نخلص من هذا أن التفاعل النووى الواحد يُخرج لنا طاقة تعادل ملايين المرات الطاقة التى يخرجها لنا أى تفاعل كيميائى. .
الاحتراق الكيميائى والاحتراق النووى
الاحتراق الكيميائى هو تفاعل كيميائى طارد للحرارة يتميز بأنه متسلسل أي أنه يغذى نفسة طالما وُجدت المواد المتفاعلة مع بعضها، وهى تشمل الأكسجين وأية مادة أخرى يمكن أن تتفاعل معه بسهولة نسميها فى العادة وقودا؛ أي أن الاحتراق هو باختصار اتحاد الوقود بالأكسجين. ويحتاج الاحتراق إلى طاقة تنشيط activation energy فى البداية، ولكنه متى بدأ يستمر من تلقاء نفسه إلى أن ينفد الوقود أو يتم إخماده بفعل فاعل. ولتوضيح ذلك نأخذ موقد البوتاجاز كمثال، فإذا أدرنا مفتاح الموقد تصاعد الوقود الغازى واختلط بالأكسجين دون أن يحدث شىء؛ فالبوتاجاز لا بد أن يصل إلى درجة حرارة مرتفعة لكى يتحد بالأكسجين ويطرد الحرارة. وهذا ما يحدثه عود الكبريت فهو يرفع درجة حرارة كمية من البوتاجاز إلى درجة الاشتعال فتشتعل وتطرد الحرارة، وتعمل هذه الحرارة المنبعثة على اشتعال كمية أخرى من البوتاجاز فتشتعل وتطرد مزيدا من الحرارة التى تعمل على اشتعال كمية أخرى من البوتاجاز، وهكذا. وبالطبع يتم تصميم الموقد بحيث يمكن التحكم فى كمية الغاز المتصاعدة لكى يكون الاحتراق تحت التحكم بحيث يمكن زيادته أو إنقاصه بتغيير كمية الغاز المتصاعدة من الصمام، وفى حالة الرغبة فى إنهاء التفاعل يقفل صمام الغاز. وهكذا يمكن تسمية هذا التفاعل "التفاعل المتسلسل chain reaction ". يحدث نفس الشئ فى الوقود النووى؛ فهناك نوع من التفاعلات النووية يسمى "الانشطار fission"، وهو انشطار نواة ذرة مادة الوقود النووى لكى تعطى نواتين مجموع كتلتيهما أقل من كتلة نواة الذرة المنشطرة، ويتحول الفرق بين كتلة المادة المنشطرة وكتلة نواتج الانشطار إلى طاقة حرارية وطاقة إشعاعية، وسنطلق على هذا التفاعل النووى تعبير "الاحتراق النووى الانشطارى"، ولكن هذا التفاعل لا يجرى فى أى كتلة من الوقود النووى من تلقاء نفسه إلا نادرا جدا، وإذا حدث فإنه يحدث لنواة واحدة كل فترة طويلة، ولكى يكون مجديا لابد لنا من إمداد الوقود النووى بالمنشط الذى يجعل التفاعل يبدأ أولا وفى نفس الوقت تهيئة الظروف لكى يكون التفاعل متسلسلا، وفى نفس الوقت أيضا إيجاد وسيلة للتحكم فى مقدار التفاعل بحيث يمكن زيادة معدله أو إبطائه أو وقفه تماما حسب الرغبة، وهذا ما يتم فى "المفاعل النووى nuclear reactor"، الذى هو عبارة عن تجهيز معين يحتوى فى قلبه على الوقود النووى المصمم بطريقة معينة ومعه المنشط وهو مصدر للنيوترونات التى تنطلق لتحدث الانشطار فى أنوية مادة الوقود، ويؤدى هذا الانشطار إلى انطلاق مزيد من النيوترونات فتحدث انشطارات جديدة فى أنوية أخرى ينتج عنها نيوترونات أخرى تؤدى إلى مزيد من الانشطار، وهكذا يصبح التفاعل متسلسلا. وستأتى مناقشة هذا الموضوع بتفصيل أكثر عند الحديث عن المفاعلات النووية. وهناك نوع ثان من التفاعلات النووية الطاردة للحرارة والتى يمكن استخدامها كمصدر هائل للطاقة تعادل ملايين المرات الطاقة النووية الانشطارية، وهى "التفاعلات الاندماجية fusion reactions" وفيها يتم اندماج بروتونين ونيوترونين لتكوين نواة هيليوم واحدة تقل فى كتلتها عن الجسيمات الأربعة المتفاعلة ويتحول فرق الكتلة إلى طاقة حسب معادلة النسبية أيضا، وهذه هى نوعية التفاعلات التى تجرى فى باطن الشمس.
الانفجار الكيميائى والانفجار النووى
إذا جرى التفاعل الكيميائى بين الوقود والأكسجين بصورة منضبطة وتحت التحكم سمى اشتعالاً burning، أما إذا جرى بدون تحكم وبسرعة كبيرة فإنه يصبح انفجاراً explosion، ونعود إلى مثال البوتاجاز السابق الإشارة إليه؛ إذا فتحنا الموقد لفترة طويلة دون إشعال الكبريت حتى يتصاعد الغاز بكمية كبيرة ثم أشعلنا الكبريت، فماذا يحدث؟ سيكون انفجارا مروعا نتيجة حدوث التفاعل بين كمية كبيرة من الوقود والأكسجين فى فترة وجيزة جدا تقل عن الثانية وتنطلق الطاقة فى هذه اللحظة الوجيزة، وهذا أيضا ما يحدث فى الديناميت حيث يتم حدوث التفاعل الكيميائى بين الأكسجين والمادة المتفجرة فى لحظة قصيرة ويتصاعد منهما كمية هائلة من الغازات والحرارة فى حيز ضيق جدا تؤدى إلى ضغط شديد يؤدى بدوره إلى الانفجار. يحدث نفس الشئ فى الانفجار النووى، ففيه يتم احتراق، أو بمعنى أدق انشطار، كتلة معينة من الوقود النووى بدن تحكم، فتنطلق كل طاقتها على هيئة حرارة وضغط وإشعاع فى جزء من الثانية فتحدت التدمير الذى يعادل ما تحدثه آلاف أو ملايين الأطنان من المواد شديدة الانفجار.
والآن، وبعد الانتهاء من هذه المعلومات المبسطة اللازمة كمدخل لفهم الوقود النووى الانشطارى، نبدأ فى المقالات التالية فى استعراض قصة اكتشاف الطاقة النووية ومن خلال ذلك سنفهم الكثير عن الوقود النووى والطاقة النووية.
ممدوح عبد الغفور حسن
رئيس هيئة المواد النووية سابقا
33442749
0105604772



ساحة النقاش